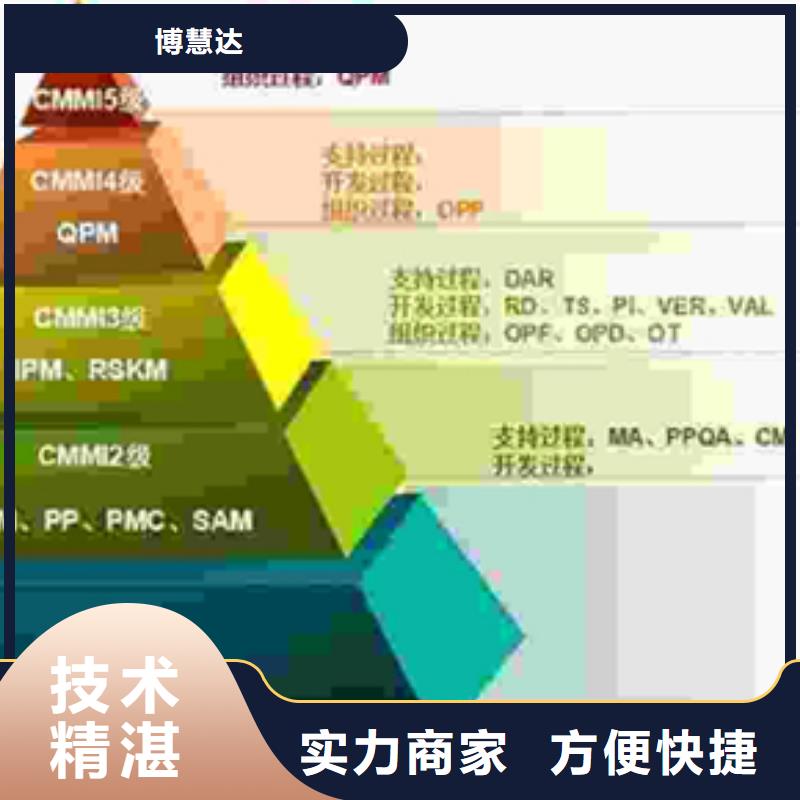
以下是:ITSS认证审核不高的产品参数
| 产品参数 | |
|---|---|
| 产品价格 | 电联/套 |
| 发货期限 | 当天 |
| 供货总量 | 999 |
| 运费说明 | 面议 |
以下是:ITSS认证审核不高的图文视频


【导语】:ITSS认证审核不高,博慧达ISO9000认证有限公司为您提供ITSS认证审核不高的资讯,联系人:宋经理,电话:13871607487、18926043348,QQ:2158148601,发货地:光明新区公明街道风景北路鑫安文化大厦发货到福建省 三明市 梅列区、三元区、明溪县、清流县、宁化县、大田县、尤溪县、沙县区、将乐县、泰宁县、建宁县、永安市。 福建省,三明市 2022年,三明市实现地区生产总值3110.14亿元,按常住人口计算,人均地区生产总值126044元。
为您精心制作的ITSS认证审核不高产品视频已准备就绪,展示产品的各项功能和特点。请您抽出片刻时间观看,相信一定会给您带来意想不到的惊喜。
以下是:ITSS认证审核不高的图文介绍

三明IATF16949认证
博慧达ISO9000认证有限公司
三明IATF16949认证的图文介绍
注重细节诚信为本

博慧达ISO9000认证有限公司于2018年在福建三明工商局注册成立,注册资本为500(万元),在公司发展壮大的4年里,我们始终为客户提供好的 福建三明IATF16949认证产品和技术支持、健全的售后服务,我公司主要经营 福建三明IATF16949认证,我们有好的产品和专业的销售和技术团队,如果您对我公司的 福建三明IATF16949认证产品服务有兴趣,期待您在线留言或者来电咨询.





产品实拍图
PRODUCT REAL SHOT DISPLAY


ISO13485认证2016对文件的要求 a)符合YY/T 0287-2017 idt ISO 13485:2016《医疗器械 质量管理体系 用于法规的要求》、GB/T ISO9001:2016/ISO 9001:2015《质量管理体系—要求》标准和《医疗器械生产质量管理规范》的要求,以及本公司实际情况的文件化质量方针和质量目标; b)质量手册; c) 产品生产和质量管理过程中,为符合YY/T0287-2017 idt ISO13485:2016《医疗器械 质量管理体系 用于法规的要求》和GB/T ISO9001:2016/ISO 9001:2015《质量管理体系—要求》标准及《医疗器械生产质量管理规范》要求所建立的各种工作程序形成的文件和记录,即程序文件; d)本公司确定的为确保其过程的有效策划、运行和控制所需的文件,包括记录; e) YY/T0287-2017 idt ISO13485:2016《医疗器械 质量管理体系 用于法规的要求》、GB/T ISO9001:2016/ISO 9001:2015《质量管理体系—要求》标准及《医疗器械生产质量管理规范》和本公司种类文件所要求的质量记录; f) 或地区法规规定的其他文件。 本公司对每一类型或型号的医疗器械建立和保持一套文档,该文档包括或识别规定产品规范和质量管理体系要求的文件,这些文件包括完整的生产过程及安装和服务过程。 4.2.2质量手册 参见本手册0.2章节。 本公司程序文件目录参见本手册9.0章节。 4.2.3 医疗器械文档 组织应为每个医疗器械类型或医疗器械族建立并保持一个或多个文档,文档包含或引用形成的文件以证明符合本标准要求和适用的法规要求。 文档的内容应包括但不限于: a)? 医疗器械的概述、预期用途/预期目的和标记,包括所有使用说明; b)? 产品规范; c)? 制造、包装、贮存、处置和流通的规范或程序; d)? 测量和监视程序; e)? 适当时,安装要求; f)? 适当时,服务程序; 4.2.4文件控制 本公司管理部组织编制《文件控制程序》以规定以下方面所需的控制: a)? 为使文件是充分与适宜的,文件发布前得到批准; b)? 必要时对文件进行评审与更新,并再次批准; c)? 确保文件的更改和现行修订状态得到识别; d)? 确保在使用处获得适用文件的有关版本; e)? 确保文件保持清晰、易于识别; f)? 确保组织所确定的策划和运行质量管理体系所需的外来文件得到识别,并控制其分发; g)? 防止作废文件的非预期使用,如果出于某种目的而保留作废文件时,应对这些文件进行适当的标识。 本公司确保文件的更改得到原审批部门或指定的其他审批部门的评审和批准,该被指定的审批部门应能获取用于作出决定的相关背景资料。 本公司至少保存一份作废的受控文件,并确定其保存期限。这个期限应确保至少在组织所规定的医疗器械寿命期内,可以得到此医疗器械的制造和试验的文件,且不少于记录或相关法规要求所规定的保存期限。 具体管理方法参见《文件控制程序》。 4.2.5记录控制 本公司为提供符合要求及质量管理体系有效运行的证据而建立的记录,应得到控制。组织应编制形成文件的程序,以规定记录的标识、贮存、保护、检索、保留和处置所需的程序。记录应保持清晰、易于识别和检索。 本公司保存记录的期限至少相当于所规定的医疗器械的寿命期,且从公司放行产品的日期起不少于2年,并且符合相关法规要求的规定。




【总结】:在福建省三明市采买ITSS认证审核不高到博慧达ISO9000认证有限公司,无论您是个人用户还是企业采购,我们都将竭诚为您服务。品质保证,价格优惠,厂家直销,欢迎有需要的客户来电。联系人:宋经理-18926043348,QQ:2158148601,地址:《光明新区公明街道风景北路鑫安文化大厦》。